合作客戶/
拜耳公司 |
同濟(jì)大學(xué) |
聯(lián)合大學(xué) |
美國(guó)保潔 |
美國(guó)強(qiáng)生 |
瑞士羅氏 |
相關(guān)新聞Info
-
> 化纖油劑配制過(guò)程與表面張力之間的影響分析
> 如何選擇卸妝油、清潔霜以及卸妝水?
> 探索泡沫粗化與表面流變學(xué)之間的關(guān)聯(lián)性疏水性蛋白——摘要、介紹
> Delta-8使用新方法測(cè)試CMC,而不是表面張力測(cè)試法——摘要
> 表面張力儀的測(cè)試方法
> 低濃度含溴鹵水中提溴:縮小氣態(tài)膜的表面張力,提高對(duì)溴的提取率
> LB膜分析儀-α-短螺旋抗菌肽對(duì)癌細(xì)胞選擇性及其抗癌作用的分子機(jī)制:結(jié)果、討論、結(jié)論、致謝!
> 探索表面張力小實(shí)驗(yàn)
> 抗抑菌洗滌劑的研究與制備
> 不同膜壓下鈣誘導(dǎo)的磷脂排序研究——摘要、介紹
推薦新聞Info
-
> 石油磺酸鹽中有效組分的結(jié)構(gòu)與界面張力的關(guān)系
> 乙醇胺與勝坨油田坨28區(qū)塊原油5類(lèi)活性組分模擬油的動(dòng)態(tài)界面張力(二)
> 乙醇胺與勝坨油田坨28區(qū)塊原油5類(lèi)活性組分模擬油的動(dòng)態(tài)界面張力(一)
> ?全自動(dòng)表面張力儀無(wú)法啟動(dòng)、讀數(shù)不穩(wěn)定等常見(jiàn)故障及解決方法
> 混合型烷醇酰胺復(fù)雜組成對(duì)油/水界面張力的影響規(guī)律(二)
> 混合型烷醇酰胺復(fù)雜組成對(duì)油/水界面張力的影響規(guī)律(一)
> 懸滴法測(cè)量液體表面張力系數(shù)的測(cè)量裝置結(jié)構(gòu)組成
> 多晶硅蝕刻液的制備方法及表面張力測(cè)試結(jié)果
> 高溫多元合金表面張力的計(jì)算方法及裝置、設(shè)備
> 納米生物質(zhì)體系性能評(píng)價(jià)及驅(qū)油特性實(shí)驗(yàn)研究
突破口服給藥遞送生理障礙,助力超長(zhǎng)效給藥
來(lái)源:藥渡 瀏覽 959 次 發(fā)布時(shí)間:2022-09-19
一、概述
口服給藥途徑是主要的藥物遞送技術(shù)之一,它也是最受患者歡迎的劑型之一。盡管口服給藥患者依從性很高,但通過(guò)口服給藥途徑的抗癌、疫苗、蛋白質(zhì)等藥物,其生物利用度是有限的。口服給藥必須克服生理障礙,如低溶解度、滲透性以及降解等,以實(shí)現(xiàn)有效和持續(xù)的給藥。
我們通過(guò)本篇文章主要介紹:口服給藥生理障礙以及克服生理障礙的一些技術(shù)手段,如納米顆粒、微乳、水凝膠、前藥、3D打印等技術(shù)手段。而通過(guò)這些技術(shù)手段,口服藥物也逐漸實(shí)現(xiàn)了從常規(guī)給藥到超長(zhǎng)效給藥的跨度。
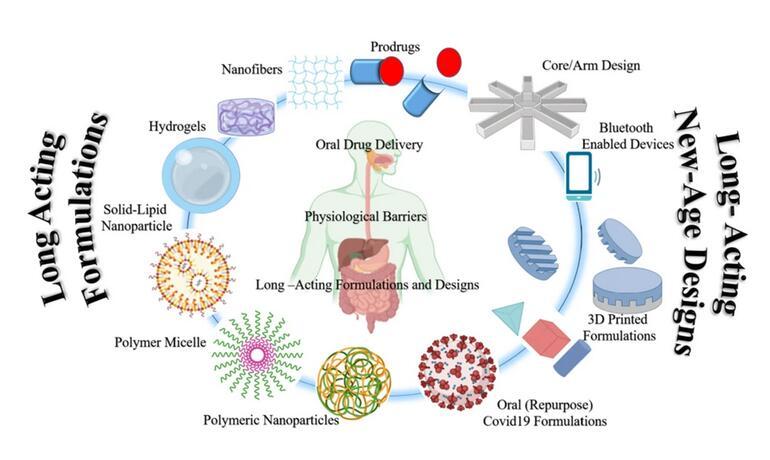
圖1.口服給藥的挑戰(zhàn)以及克服這些挑戰(zhàn)的技術(shù)設(shè)計(jì)
二、口服給藥的生理障礙及注意事項(xiàng)
1、口腔、食道以及胃粘液
口腔的唾液腺是口服制劑遇到的第一個(gè)障礙,口腔內(nèi)存在一些酶,如唾液淀粉酶,可能導(dǎo)致藥物降解。但是由于藥物在口腔內(nèi)存留時(shí)間較短,所以,一般口腔內(nèi)的障礙對(duì)藥物吸收影響較小。
食道不參與消化或藥物吸收,而是幫助藥物的轉(zhuǎn)運(yùn),它通過(guò)蠕動(dòng)將藥物推向胃部。
胃中脂肪消化酶的存在,如脂肪酶,也會(huì)導(dǎo)致藥物的水解。
酶降解阻礙了藥物的溶解,如果溶解度降低,有效藥物濃度會(huì)發(fā)生變化,從而影響藥物的吸收。如果藥物在不同的pH值下具有不同的溶解度,則在胃內(nèi)也可能發(fā)生沉淀或過(guò)飽和。一旦藥物穿過(guò)這些生化屏障(pH和酶),藥物的腸道滲透性進(jìn)一步?jīng)Q定了它的“命運(yùn)”。
2、小腸以及結(jié)腸
口服藥物在經(jīng)歷胃部的生理障礙后到達(dá)小腸。在小腸(十二指腸)的入口處,胰酶會(huì)引發(fā)幾種酶促轉(zhuǎn)化,這些酶還可能導(dǎo)致首過(guò)代謝,從而導(dǎo)致藥物生物利用度降低。因此,口服藥物必須克服這些生理學(xué)障礙。
小腸黏膜具有絨毛,腸上皮中的絨毛在藥物吸收中起著至關(guān)重要的作用,因?yàn)樗黾恿烁哌_(dá)300m2的表面積,從而促進(jìn)了藥物的吸收。口服給藥的藥物,可以通過(guò)跨細(xì)胞或細(xì)胞旁途徑被吸收。由于存在脂質(zhì)細(xì)胞膜,疏水性藥物更喜歡跨細(xì)胞途徑,而親水性分子通過(guò)細(xì)胞旁途徑轉(zhuǎn)運(yùn)。
此外,胃腸道的生物膜具有親水性頭部和親油性尾部。脂質(zhì)雙分子層阻礙了藥物分子通過(guò)細(xì)胞膜的自由運(yùn)動(dòng)。通常,分子量越高,被吸收的機(jī)會(huì)就越小。藥物分子上的電荷,也決定了其吸收的機(jī)會(huì)。由于粘蛋白帶負(fù)電荷,帶正電荷的分子可能會(huì)由于靜電相互作用而粘附。
藥物在結(jié)腸中的最終吸收,受到其溶解度和非特異性相互作用的限制。這里的非特異性相互作用,是指藥物粘附在結(jié)腸中的糞便、粘液或其他分泌物上。由于結(jié)腸會(huì)吸收水分,因此與疏水性藥物相比,親水性藥物更容易被吸收。因此,口服給藥途徑的主要挑戰(zhàn)是難溶性高分子藥物的配方,因?yàn)樗鼈內(nèi)菀资艿矫附到獠⑶液茈y被吸收。
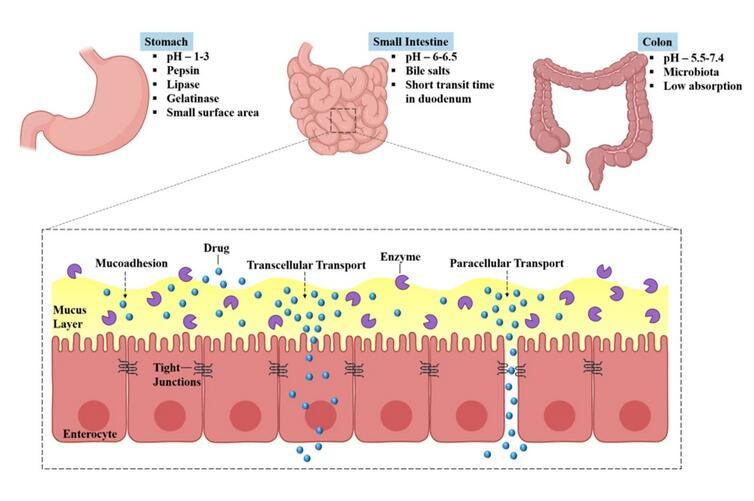
圖2.口服給藥生理障礙
三、增強(qiáng)藥物生物利用度策略
為了克服上述的生理障礙,目前有幾種技術(shù)用來(lái)克服口服藥物生理障礙,從而提高藥物的吸收及生物利用度,如納米制劑以及水凝膠等技術(shù)手段。
1、納米顆粒
納米顆粒的高表面積體積比,提高了藥物的溶解性和穩(wěn)定性。納米粒的粒徑范圍一般為100~1000nm。藥物可以被包裹在納米顆粒中以獲得持續(xù)釋放,進(jìn)而保護(hù)藥物,免受劇烈的pH值變化和胃腸道惡劣的酶環(huán)境的影響。納米顆粒的大小、形狀、表面電荷會(huì)影響藥物的藥代動(dòng)力學(xué)。
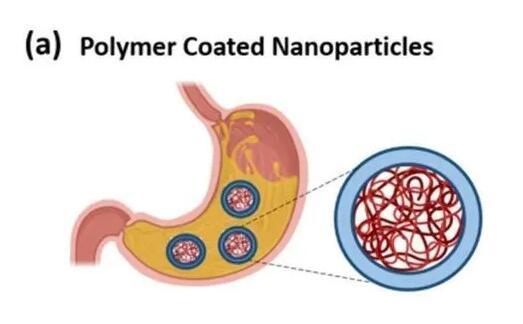
圖3.納米顆粒
受pH影響的羧基納米顆粒是口服藥物傳遞系統(tǒng)的福音,羧酸離子在酸性pH下不會(huì)電離,從而保護(hù)藥物免受惡劣環(huán)境的影響,并在腸道環(huán)境時(shí)提供針對(duì)性釋放。Eudragits是此技術(shù)常用的共聚物,廣泛用于提高親脂性藥物的生物利用度。
2、水凝膠
水凝膠是通過(guò)物理或化學(xué)交聯(lián)方法形成的三維聚合物網(wǎng)格。網(wǎng)格之間留有一定的空間,由于該網(wǎng)格的存在,水凝膠的結(jié)構(gòu)富含多孔性。聚合物網(wǎng)格可以截留大量的水,并防止其運(yùn)輸?shù)酵獠凯h(huán)境,從而模仿生物組織的物理特性。這種保水能力,使水凝膠能夠提供良好的生物相容性和封裝藥物分子的平臺(tái)。該網(wǎng)格可以限制不同酶的滲透,從而保護(hù)包封的藥物免受各種酶降解。
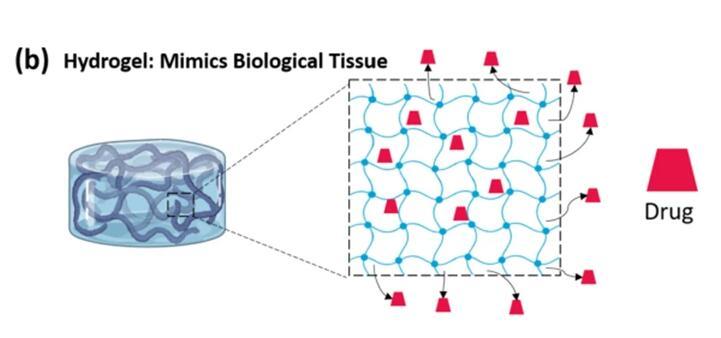
圖4.水凝膠
四、口服制劑長(zhǎng)效給藥
1、前藥技術(shù)
前體藥物是活性藥物分子的無(wú)活性或活性較低的生物可逆轉(zhuǎn)衍生物,在產(chǎn)生藥理作用之前,需要經(jīng)過(guò)酶或生物轉(zhuǎn)化。前藥策略提高了許多分子的性能,它有助于增強(qiáng)口服給藥后的藥物吸收以及穩(wěn)定性。前藥在市場(chǎng)中一直占據(jù)著一席之地,而且發(fā)展迅速,以下為FDA批準(zhǔn)的一些長(zhǎng)效前藥:
表1.FDA批準(zhǔn)的長(zhǎng)效前藥

但前藥技術(shù)也還有一些挑戰(zhàn)需要克服。它涉及復(fù)雜的化學(xué)反應(yīng),因?yàn)榭刂妻D(zhuǎn)化部位可能很麻煩,并且前藥中活性藥物的釋放可能還涉及副產(chǎn)物的,每個(gè)產(chǎn)物的毒性評(píng)估都至關(guān)重要。
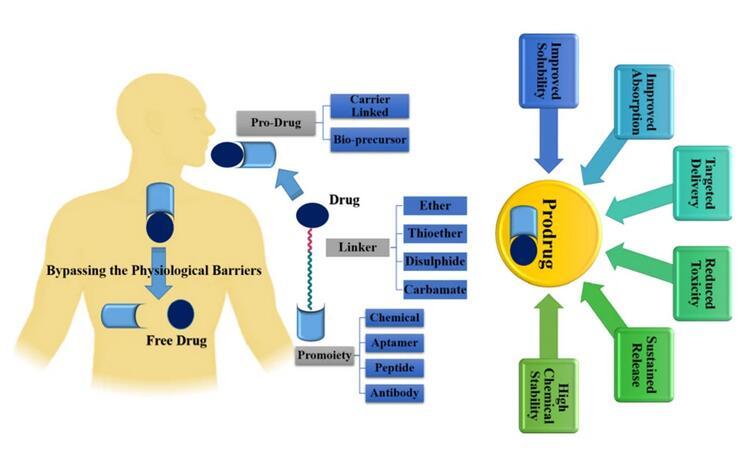
圖5.前藥方法
2、3D打印
3D打印技術(shù)中不需要造粒、壓片以及包衣等環(huán)節(jié),并且可以靈活控制藥物的劑量以及釋放,所以該技術(shù)逐漸發(fā)展起來(lái)。3D打印技術(shù)主要有選擇性激光燒結(jié)(SLS)、光固化成型(SLA)、熔融沉積成型(FDM)、半固體擠出成型(SSE)以及噴墨成型打印(IJP)等方式。3D打印藥物目前的代表藥物,為FDA批準(zhǔn)的Spritam。
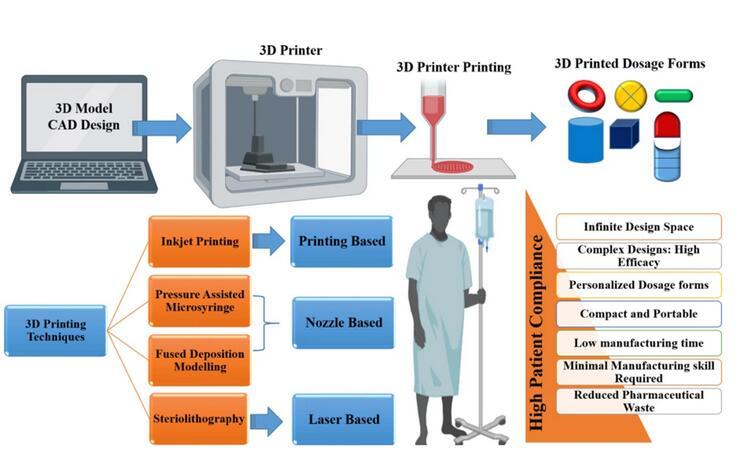
圖6.3D打印技術(shù)
五、總結(jié)
隨著納米技術(shù)和3D打印的發(fā)展,口服制劑取得了長(zhǎng)足的進(jìn)步。長(zhǎng)效以及超長(zhǎng)效口服藥物的開(kāi)發(fā),是研究人員和科學(xué)家研究的重點(diǎn)。藥代動(dòng)力學(xué)研究表明,超長(zhǎng)效釋放具有減少副作用和提高患者依從性的潛力。
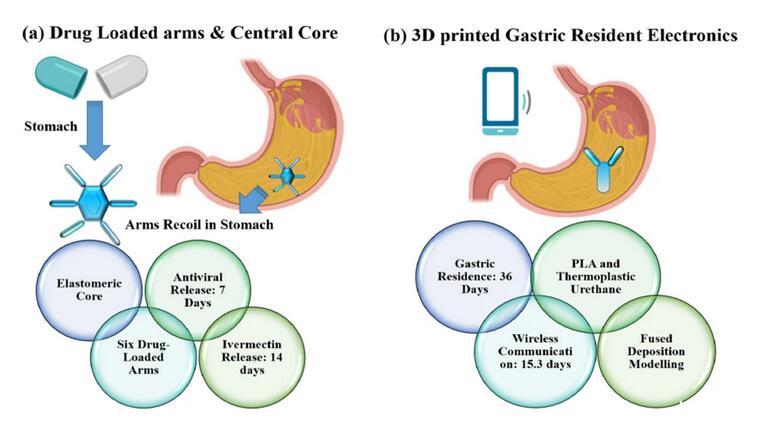
圖7.兩種超長(zhǎng)效給藥設(shè)計(jì)
科學(xué)不斷發(fā)展,技術(shù)不斷更迭,相信未來(lái)我們可以實(shí)現(xiàn)口服藥物的更長(zhǎng)效的釋放,并且具有更高的生物利用度。
今天的分享就到這里,小編水平有限,如有不足,歡迎各位同仁批評(píng)指正。
參考文獻(xiàn):
[1]Sato Y,Joumura T,Takekuma Y,et al.European Journal of Pharmaceutics and Biopharmaceutics[J].European Journal of Pharmaceutics and Biopharmaceutics,2020,154.
[2]季文.口服結(jié)腸定位給藥系統(tǒng)研究進(jìn)展[J].臨床醫(yī)藥實(shí)踐,2006,15(10):4.










